معرفی عناصر پرتوزا در جدول تناوبی| مواد رادیواکتیو چه کاربردهایی دارند؟

عناصر پرتوزا، موادی هستند که امواج رادیواکتیو مانند امواج آلفا، بتا و گاما را ساطع میکنند. این مواد در سراسر پوسته زمین یافت میشوند و کاربردهای مهمی در زمینههای مختلف از جمله دارو، تولید انرژی و ... دارند. عناصر رادیواکتیو به دلیل وجود بار هستهای اضافی در هسته اتمی خود، ناپایدار هستند. این هستههای اتمی برای تشکیل هستههای پایدار، دچار فروپاشی میشوند. عناصری که تحت واپاشی رادیواکتیو قرار میگیرند، پرتوزا نامیده میشوند.
به تعبیری دیگر، برخی از عناصر به دلیل بار بیش از حد متمرکز در هسته، در طبیعت پایدار نیستند و از آنجا که همه عناصر میخواهند در طبیعت پایدار باشند، دچار واپاشی رادیواکتیو میشوند. عناصری که تحت واپاشی رادیواکتیو قرار میگیرند، عناصر پرتوزا هستند.
در این مقاله با عناصر پرتوزا در جدول تناوبی، ویژگیها و کاربردهای آنها بیشتر آشنا میشویم.
ساختار عناصر پرتوزا در جدول تناوبی
در اتمهای پایدار، نسبت نوترون به پروتون در هسته، معمولاً نزدیک به 1:1 است (Z<20). با این حال، در ایزوتوپهای ناپایدار یا رادیواکتیو، این نسبت ممکن است به طور قابل توجهی متفاوت باشد که میتواند بر ثبات و رفتار فروپاشی آنها تأثیر بگذارد. این نسبت معمولاً با افزایش عدد اتمی افزایش مییابد. با این حال چند استثنا هم وجود دارد، مثلا (Protium) و (Helion) که هر دو پروتون بیشتری نسبت به نوترون دارند و همچنان پایدار هستند.
تاریخچه عناصر رادیواکتیو
در سال 1896، هانری بکرل، فیزیکدان فرانسوی، در حالی که در حال بررسی ارتباط بین فسفرسانس و اشعه ایکس بود، رادیواکتیویته خود به خودی را در نمکهای اورانیوم کشف کرد. بکرل در زمینه فلورسانس و فسفرسانس مطالعه میکرد، موضوعی که پدرش در آن متخصص بود. او دریافت که نمکهای اورانیوم بدون هیچگونه تحریک نور خورشید، تشعشعات ساطع میکنند. کشف بکرل تصادفی اما مهم بود و منجر به مطالعه سایر عناصر رادیواکتیو توسط ماری کوری و پیر کوری شد که اصطلاح "رادیواکتیویته" را ابداع کردند.
فهرست عناصر پرتوزا در جدول تناوبی
عناصر رادیواکتیو مختلفی در جدول تناوبی وجود دارد. به طور کلی تعداد عناصر پرتوزا در جدول تناوبی عناصر شیمیایی، 37 عدد است. برخی از آنها طبیعی و برخی دیگر ساخته دست بشر هستند.
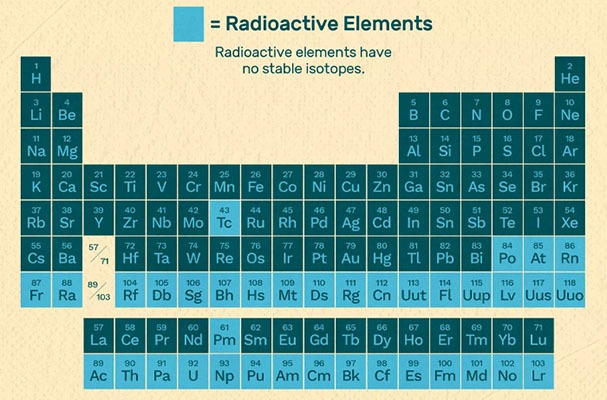
فهرست عناصر پرتوزای طبیعی
عناصر رادیواکتیو بسیار کمی وجود دارند که به طور طبیعی به وجود میآیند؛ زیرا این مواد بسیار ناپایدار هستند و تمایل دارند خیلی سریع به عناصر دیگر تجزیه شوند. برخی از عناصر پرتوزای طبیعی عبارتند از:
اورانیوم
اورانیوم با عدد اتمی 92 و نماد U یک عنصر رادیواکتیو طبیعی است که در خاک، هوا و آب وجود دارد. اورانیوم به طور پیوسته به عناصر دیگری مانند رادیوم و رادون تجزیه میشود. ایزوتوپهای مختلفی از اورانیوم وجود دارد، اما فراوانترین ایزوتوپ U-238 است که تقریباً 99 درصد کل اورانیوم موجود در زمین را تشکیل میدهد.
پولونیوم
پولونیوم عنصری نادر و پرتوزا با عدد اتمی 84 و نماد Po است. ماری و پیر کوری در سال 1898 آن را کشف کردند و به نام کشور لهستان نامگذاری کردند. پولونیوم مادهای بسیار سمی میباشد و پایدارترین ایزوتوپ آن پلونیوم 210 است. این ماده به طور طبیعی در مقادیر کم در پوسته زمین وجود دارد، اما میتواند به طور مصنوعی در راکتورهای هستهای نیز تولید شود.
رادیوم
رادیوم یک عنصر فلزی کمیاب و بسیار پرتوزا است که در اورانیوم و توریم در سطوح کمی یافت میشود. رادیوم که در سال 1898 کشف شد، پرتوهای آلفا، بتا و گاما ساطع میکند و یکی از ناپایدارترین عناصر است.
رادون
رادون یک عنصر شیمیایی با عدد اتمی 86 و نماد Rn است. این گاز رادیواکتیو بیرنگ، بیبو و بیمزه، به طور طبیعی توسط تجزیه رادیوم تولید میشود. رادون سلامتی انسان را تهدید میکند؛ زیرا دومین عامل سرطان ریه بعد از سیگار است.
ویژگیهای عناصر رادیواکتیو
عناصر پرتوزا دارای چندین ویژگی هستند، از جمله:
- از آنجا که در هستههایشان مقدار زیادی پروتون یا نوترون دارند، ناپایدار هستند و میتوانند تجزیه شوند.
- آنها پرتوهای رادیواکتیو ساطع میکنند، یعنی تحت واپاشی رادیواکتیو قرار میگیرند.
- تشعشعات ساطع شده از این عناصر بسیار سمی است.
- آنها میتوانند تحت سه نوع واپاشی رادیواکتیو قرار گیرند: تجزیه آلفا، بتا و گاما.
- دامنه ذرات بتا بالاتر از آلفا و کمتر از پرتوهای گاما است.
- قدرت نفوذ ذرات بتا کمی بیشتر از آلفا اما کمتر از پرتوهای گاما میباشد.
موارد استفاده از عناصر رادیواکتیو
کاربردهای مهم متعددی برای عناصر رادیواکتیو وجود دارد، از جمله:
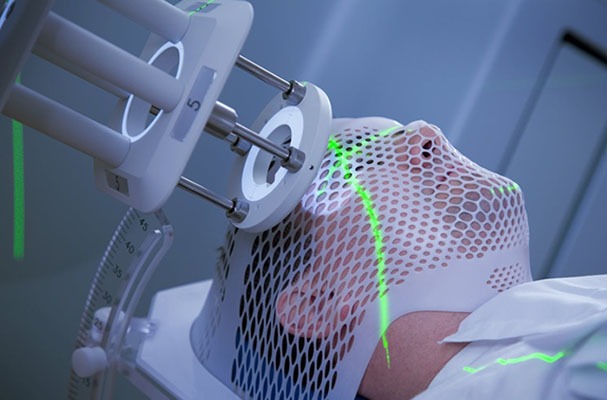
- تشخیص و درمان پزشکی: ایزوتوپهای رادیواکتیو در رادیوتراپی و تصویربرداری پزشکی برای شناسایی و درمان بیماریهایی مانند مشکلات تیروئید و سرطان استفاده میشوند. عنصر رادیواکتیو که در درمان سرطان استفاده می شود، رادیوم است.
- کاربردهای علمی و صنعتی: ایزوتوپهای رادیواکتیو در کاربردهای علمی متعددی مانند رادیوگرافی، مطالعات ردیاب و آنالیز مواد به کار میروند.
- کاربردهای تاریخی: ایزوتوپهای رادیواکتیو همچنین برای تاریخیابی سنگها و فسیلها استفاده میشوند و به دانشمندان اجازه میدهند تا تاریخ زمین و تکامل حیات را بهتر درک کنند.
- تولید انرژی: تاسیسات انرژی هستهای با استفاده از ایزوتوپهای رادیواکتیو مانند اورانیوم برق تولید میکنند.
- آشکارسازهای دود: آشکارساز دود دارای مقدار کمی مواد رادیواکتیو در داخل است که هوا را یونیزه میکند و زمانی که ذرات دود شناسایی میشوند، زنگ هشدار به صدا در میآید.
- نگهداری غذا: با استفاده از اشعه برای از بین بردن باکتریها و سایر میکروبها، میتوان غذا را تازه نگه داشت و از فاسد شدن آن جلوگیری کرد.
تاثیرات عناصر پرتوزا
اثرات این عناصر به نوع و انرژی تشعشعات ساطع شده از آنها بستگی دارد. اگر فردی برای مدت طولانی در معرض این اشعهها قرار گیرد، مستعد ابتلا به سرطان است؛ اما این اتفاق تنها پس از چندین سال قرار گرفتن در معرض آنها برای ساعات طولانی رخ میدهد. مواد پرتوزا به دلیل ایجاد آسیب سلولی و سوختگی بسیار خطرناک هستند.
قرار گرفتن در معرض مقادیر زیادی از عناصر پرتوزا، میتواند باعث ریزش مو، حالت تهوع، استفراغ، خونریزی، اسهال، آسیب به سیستم عصبی مرکزی و ... شود. این مواد خطر ابتلا به سرطان و آسیب DNA را به ویژه در جنینها و کودکان خردسال افزایش میدهند. همچنین در برخی موارد شدید میتوانند منجر به مرگ شوند. توصیه میشود در هنگام کار در اطراف عناصر رادیواکتیو همیشه مراقب باشید و از کیتهای محافظ استفاده کنید تا از خطر اثرات مضر آنها جلوگیری شود.

